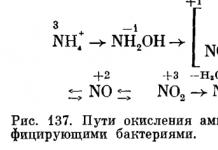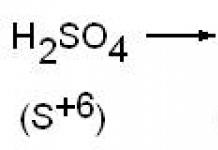Евгений Грановский
Этот материал, замысленный еще в стародавние времена, до создания этого сайта, оказался для меня настоящей ловушкой. Активная позиция на интернет-форумах требовала каждый раз писать слишком много слов, хотелось скомпоновать и систематизировать информацию, чтобы потом просто ссылаться. На деле же это означало новый уровень погружения в тусклый мир патрубков и губок вместо того, чтобы писать о диковинных тропических рыбах и далеких биотопах. И, в итоге, я вовсе перестал что-либо писать. Материал наверное бы так и остался у меня в компьютере, если бы Сергей Аникштейн не сподвиг меня довести работу до какого-то более или менее читаемого состояния и, собравшись с духом, так опубликовать. Текст, несмотря то, что в него добавлен ряд новых параграфов, изрядно сырой. Кое-какие моменты мне и самому по прошествии лет кажутся спорными или, как минимум, требующими дополнительной проверки. Впрочем, аквариумистика – это не та область, где может и должно быть единственно правильное мнение, и подчас противоположные решения приводят в нашем деле к одинаково хорошему результату. В любом случае, думаю, что представленный материал окажется хорошим отправным пунктом для аквариумиста, который хочет разобраться в этих вопросах. Но самое главное здесь – это не впасть в излишний технофетишизм, ибо на свете существует еще очень много всего, гораздо более интересного и занимательного, чем химические реакции, фильтры и помпы.
* * *
В современной аквариумистике фильтры являются одним из важнейших средств жизнеобеспечения. Аквариум - замкнутое биологическое пространство, в котором происходит постоянное накопление органических остатков: рыбы производят выделения, которые загрязняют воду; плюс несъеденный корм, помертвевшие части растений и т.д. В природных водоемах концентрация отходов в воде достаточно стабильна, поскольку часть их перерабатывается в минеральные вещества и ассимилируется растениями, а другая часть выносится вместе с водными потоками. В аквариуме плотность посадки рыб существенно превышает природную, поэтому продукты обмена и их неорганические производные могут оказывать негативное воздействие на его обитателей.
Основными способами удаления из аквариума излишков минеральных и органических остатков и налаживания в нем приемлемых условий жизни рыб является фильтрация, чистка, подмены воды и применение сорбирующей химии.
Наряду с навыками обращения с фильтрующими системами, помпами, сифонами и абсорбентами аквариумист должен обладать также определенным объемом теоретических знаний. Неотъемлемой частью современной аквариумной науки является так называемый "азотный цикл". Если вы откроете старые книжки, то не найдете там ни слова ни о биофильтрах, ни об азотном цикле. Первого тогда просто не существовало, второе же протекало само собою, о чем аквариумисты "старой школы" лишь смутно догадывались говоря об неком "биологическом равновесии", которое наступает само собой через несколько недель после запуска. То, как правило, были густо заросшие аквариумы с нейтральной или подкисленной водой, населенные "харацинкой" или "живородкой", где живые растения достаточно энергично поглощали ядовитые аммонийные соединения, а если те и присутствовали в незначительных остаточных дозах, то преимущественно в виде относительно безопасных ионов аммония NH 4 +. Более того, в "голландские аквариумы", с большим количеством растений и малым числом рыб, нитраты вносились искусственно!
Увлечение цихлидами, захватившее аквариумистику начиная с 1970-х годов, потребовало от аквариумистов намного более углубленных знаний в области биофильтрации. Хотя до того этот сегмент был уже в значительной мере освоен морскими аквариумистами. Именно они первыми столкнулись с проблемой ядовитых нитрогенов и стали разрабатывать соответствующие системы водоочистки. Вслед за "моряками" и цихлидоводами на эту проблему обратили и другие аквариумисты, а производство аквариумных фильтров превратилось в целую отрасль аквариумной индустрии.
В настоящем материале обобщены и систематизированы личный практический опыт и информация, почерпнутая в различных источниках. Их список приведен в конце. Хочу поблагодарить всех, чьи публикации и высказывания на аквафорумах помогли мне в составлении этого материала.
Азотный цикл, нитрификация
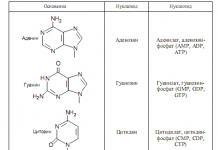
Не съеденный корм и выделенные с экскрементами не потребленные рыбой белки - это основные поставщики органических соединений в воде, в которой начинается цикл биологических превращений, осуществляемых различными микроорганизмами. На первом этапе этого цикла сложные азотсодержащие органические соединения утилизируются до простых неорганических - так называемая минерализация. Азот - один из основных элементов, необходимых для животных и растений. Он входит в животные и растительные белки. В результате разложения экскрементов рыб, остатков корма и растений, погибших организмов образуется аммиак NH 3 (ammonia). Аммиак обладает способностью взаимодействовать с ионами водорода H + , находящимися в воде, или с молекулами воды, образуя ионы аммония NH 4 + (ammonium):
NH 3 + H + = NH 4 +
2NH 3 + 3O 2 = 2NO 2 - + 2H + + 2H 2 O,
либо 2NH 4 + + 3O 2 = 2NO 2 - + 4H + + 2H 2 O,
а затем в нитрат-ионы (с буквой "а") NO 3 - .
2NO 2 - + O 2 = 2NO 3 - .
Процессы окисления аммиака и ионов аммония до нитрит-ионов, а затем до нитрат-ионов называются нитрификацией. Эти процессы протекают в аэробной (т.е. богатой кислородом) среде под действием бактерий-нитрификаторов, существующих в аквариуме. Практический смысл нитрификации заключается в переводе соединений азота из очень токсичных форм (аммиак, нитрит) в малотоксичную (нитрат). Нитраты - тоже вредны, однако не настолько, как предыдущие соединения азота. Но на этом цикл азота не прекращается. Существует и обратный - восстановительный процесс, называемый денитрификацией, который мы, в большинстве своем, на настоящий момент не используем. Потому в аквариумной практике азотный цикл чаще всего рассматривается в только в аспекте нитрификации. В этом аспекте современная аквариумистика фактически построена на принципе "пролонгированной протоки", т.е. нитрат выводится из аквариума посредством замены загрязненной воды на свежую. Также существенную роль играют живые растения, поглощающие нитраты. В цихлидом аквариуме, где растительности мало или она вовсе отсутствует, биологическое равновесие биосистемы и здоровье рыб во многом зависит от технического оснащения и регулярности обслуживания. Хорошая аэрация и фильтрация является обязательным условием нормального функционирования такой системы, а поддержание концентрации нитратов на безопасном уровне осуществляется посредством интенсивных вливаний свежей воды. Несмотря на существование ряда альтернативных решений (включая биологические методы денитрификации, о которых будет рассказано в третьей части статьи), ведра и шланги являются неотъемлемым аквариумным инвентарем.
Токсичность азотных соединений
Сам по себе газообразный азот, молекулы которого состоят из двух атомов N 2 , химически и биологически инертен и практически безвреден. А вот азотные соединения, накапливающиеся в аквариуме, способны нанести вред его обитателям. Схематически изменение концентраций соединений азота в аквариуме в процессе нитрификации и изображено на графике.
|
Изменение концентраций соединений азота в аквариуме |
Согласно "Перечню рыбохозяйственных нормативов предельно допустимых концентраций
(ПДК) и ориентировочно безопасного уровня воздействия (ОБУВ) вредных веществ
для воды водных объектов, имеющих рыбохозяйственное значение" (М.: Изд.
ВНИРО, 1999), ПДК азотных соединений для рыб:
аммиак - 0,05 мг/л;
аммоний - 0,5 мг/л;
нитрит - 0,08 мг/л (значение нитритно-азотной концентрации);
нитрат - 40 мг/л.
Хотя практика показывает, что аквариумные рыбы кратковременно способны переносить значительно более высокие дозы нитрогенов, эти значения не следует превышать.
Аммиак является сильно токсичным соединением. Он легко попадает в кровь и внутренние органы рыбы, накапливается там и потом выводится очень долго, вплоть до недель, т.е. рыба единожды отравившаяся аммиаком может через какое-то время погибнуть, причем без всяких внешних признаков. Отравления аммиаком также делает рыб подверженными стрессу и ослабляет их сопротивляемость болезням. Летальный уровень неионизированного аммиака составляет примерно 0,2–0,5 мг/л для различных видов рыб. Ионы аммония тоже токсичны, но в меньшей степени. Токсичность аммиака уменьшается в соленой воде. Соотношение концентраций NH 3 и NH 4 + в воде также зависит от ее кислотности и температуры: в кислой и холодной воде аммиак практически отсутствует, в щелочной и теплой среде его концентрация возрастает. Поэтому в аквариумной литературе советуют подкислять воду для предотвращения отравления рыб. Понижение pH действительно приводит к снижению токсичности аммиака, однако при этом активность нитрифицирующих бактерий, перерабатывающих аммиак падает. А при pH ниже 5, их жизнедеятельность практически прекращается.
Проблема усугубляется тем, что имеющиеся в нашем распоряжение тесты показывают общую концентрацию аммонийных соединений, не отделяя аммиак от аммония. Их процентное соотношение можно определить, используя специальные таблицы, исходя из показателей pH и температуры воды. Но лучше всего устроить фильтрацию так, чтобы тест показывал нулевое значение.
Существующее однако мнение, что при значениях рН=7 и менее риск вероятность аммиачного отравления является практически нулевым. В подтверждение чего указывается, что в "доцихлидную" эпоху, когда аквариумисты содержали преимущественно тропических "кисловодных" рыб, случаи отравлений аммиаком были очень редки, и эта проблема возникла только с наступлением "моды" на африканских цихлид, требующих щелочной воды. На мой взгляд, это неверная аргументация, т.к она не принимает во внимание тот существенный момент, что в прежние времена все аквариумы, в т.ч. выростные, в обязательном порядке содержали растения, которые и выполняли роль естественного биофильтра и аэратора, причем довольно успешно. Тем более, как выше указано, ионы аммония тоже не безвредны и при накапливании могут вызвать длительное отравление.
Отдельной проблемой является наличие аммонийных соединений (далее по тексту мы будем называть их обобщенно "аммиак") в водопроводной воде - в период осенних дождей и весеннего паводка концентрация может достигать 0,5–1 мг/л. Более детально это рассмотрено в статье " ". Причем здесь аммиак опасен даже не столько своей абсолютной концентрацией, сколько резким скачком его содержания в аквариуме при обильной подмене воды.
Нитрит также ядовит. Длительное пребывание рыб в воде с нитритно-азотной концентрацией более 0,1 мг/л (или общей нитритно-ионовой концентрацией более 0,33 мг/л) нежелательно, летальными могут оказаться дозы от 1 мг/л.
Примечание: существуют две измерительные шкалы содержания нитрита: общей нитритно-ионовой концентрации (NO 2 -), т.е. содержание азота и кислорода; и нитритно-азотной концентрации (NO 2 – N), т.е. содержание только азота в нитрит-ионе. Коэффициент соотношения этих показателей равен 3,3, то есть, зная одно значение, можно вычислить другое. В книгах обычно указывается показатель нитритно-азотной концентрации, а вот в аквариумных тестах - как правило общей нитритно-ионовой.
Хочу еще раз подчеркнуть - в нормально функционирующем аквариуме содержание аммиака и нитрита должно быть нулевым.
Нитраты - значительно менее токсичны, чем аммиак и нитриты. Безопасной для большинства видов рыб считается концентрация ионов NO 3 - до 50 мг/л. Хотя известны случаи аквариумов с содержанием нитрата до 400 мг/л (!!!), что ни в коем случае не должно рассматриваться как рекомендация к действию. В тоже время, существуют виды цихлид, например, у дикарей Uaru fernandezyepezi самочувствие ухудшается уже при концентрации 10-20 мг/л. Однако даже если мы не видим очевидных признаков отравления или ухудшения самочувствия, рыба внешне здорова и нерестится, в долговременном аспекте нитраты являются одной из главных причин гексамитоза и др. заболеваний у проблемных видов и возрастных рыб и оказывают воздействие даже более вредное, чем неправильное кормление, хотя негативный их эффект проявляется не сразу. Даже в относительно небольших и формально "безопасных" концентрациях нитраты незаметно, но верно укорачивают срок жизни нашим питомцам. Также есть основания предположить наличие токсичного "кумулятивного эффекта" при сочетании с нитратов с нитритным или аммонийным фоном (при недостаточной биофильтрации). Поэтому и для сравнительно неприхотливых видов, лучше установить такой режим подмен воды, чтобы концентрация NO 3 - была минимальной. Следует также избегать резких изменений концентрации нитратов не только в большую сторону, но и в меньшую, в частности, при пересадке рыб в другую емкость или при больших подменах воды.
Симптомы отравления рыб азотными соединениями достаточно хорошо описаны в литературе. В частности, об этом можно прочесть в статье "Состав аквариумной воды: основные проблемы" , размещенной на веб-сайте vitawater.ru. Оттуда же можно узнать, как с помощью специальных препаратов, как фирменных, так и "народных" (соль, марганцовка, метиленовая синь) улучшить самочувствие рыбок. Однако если изначально сделать все по уму: оснастить аквариум хорошим фильтрационным оборудованием и обеспечить должный режим обслуживания, т.е. устранить причину "заболевания", не будет нужды бороться с его симптомами.
Виды фильтрации
Основное назначение аквариумных фильтров - очистка воды, удаление из нее нежелательных составляющих (органических и минеральных частиц, молекул, ионов, микроорганизмов). Фильтрацию можно разделить на три основных вида:
Механическая;
- биологическая;
- химическая.
Механическая фильтрация - улавливание взвешенных в воде частиц. При механической фильтрации поток воды проходит через какой-либо мелкопористый материал, на котором задерживаются сравнительно крупные частички грязи и аквариумного мусора. В качестве фильтрующего субстрата обычно применяются синтетические губки и мочалки, специальный поролон, синтепон и т.д.
Теоретически, эффективность очистки возрастает при уменьшении размера частиц фильтрующего материала или диаметра проходных каналов. Однако это уменьшение возможно лишь до определенных пределов, поскольку при этом начинает возрастать сопротивление потоку жидкости и снижается производительность фильтра. Считается, что лучше применять фильтрующие элементы с различной величиной проходных каналов. Вода, последовательно минуя слои со все уменьшающимися каналами, будет равномерно очищаться во всем объеме фильтра. Во внешних и в некоторых видах внутренних фильтров используется многослойный фильтрующий элемент (керамические кольца - крупнопористые и мелкопористые губки - синтепон). При работе механического фильтра в нем происходит накопление отфильтрованного материала, поэтому необходимо регулярно проводить промывку фильтрующего элемента.
К механической фильтрации можно и отнести и регулярную чистку дна сифоном (сифонка грунта) при подменах воды.
Биологическая фильтрация - многостадийный, многоступенчатый процесс, осуществляемый аммонифицирующими и нитрифицирующими, по разложению органики и преобразованию сильнотоксичных аммиака, аммония и нитрита в малотоксичный нитрат (а при полном цикле - в газообразные азот). Этот процесс может протекать естественным образом непосредственно в аквариуме, но для получения хорошего результата требует специального устройства - биофильтра.
Биологическая и механическая фильтрация тесно между собой связаны. Во-первых, потому, что один и тот же фильтр может выполнять роль и механического, и биологического. Во-вторых, тем, что задача очистки аквариума от органических нечистот решается одновременно как в биологически, посредством нитрификации, так и механически, т.е непосредственно удалением грязи из аквариума. И таким образом сильная механическая фильтрация ослабляет нагрузку, ложащуюся на биофильтр, и наоборот.
Химическая фильтрация , под которой в аквариумной практике понимают прежде всего сорбцию , является специфичным видом. С помощью химических фильтров из аквариумной (или вновь заливаемой) воды удаляются вредные органические и неорганические вещества, а также могут изменяться параметры воды и вноситься в нее полезные вещества. В зависимости от характера сорбции различают адсорбенты - тела, поглощающие вещество на своей (обычно сильно развитой) поверхности, и химические поглотители, которые связывают поглощаемое вещество, вступая с ним в химическое взаимодействие. Отдельную группу составляют ионообменные сорбенты, поглощающие из растворов ионы одного типа с выделением в раствор эквивалентного количества ионов другого типа. Химическая фильтрация наиболее распространена и популярна с помощью активированного угля в качестве адсорбента. Применяется и ряд других химических наполнителей. Это минералы из группы цеолитов, синтетические ионообменные смолы, а также торф. Цеолиты и ионообменные смолы поглощают аммиак, нитраты, фосфаты и др. и вместо них выделяют безвредные ионы натрия, хлора, сульфата и т.д. Торф слегка подкисляет воду и вносит в нее различные биологически активные вещества. К химической фильтрации можно отнести и пеноотделительные колонки, которые удаляют органические молекулы из воды прежде, чем они будут разложены с выделением аммиака. Озонаторы тоже в какой-то степени выполняют химическую фильтрацию путем окисления органики.
Кроме фильтрации, в аквариумной практике применяется также стерилизация воды как метод ее очистки. Способами стерилизации являются озонирование и ультрафиолетовое облучение.
Нитрифицирующие бактерии
Процесс нитрификации - это процесс окисления, основную роль в котором, естественно, играет кислород. Однако этот процесс происходил бы намного медленнее, не будь в аквариуме множества микроорганизмов, принимающих в нем участие. Эти микроорганизмы известны также под собирательным названием "активный ил ".
Предварительную работу делают минерализаторы, превращающие органику в аммиак. Такой способностью обладают многие микроскопические водные обитатели. Поэтому, в принципе, набор видов может быть свой для каждого конкретного аквариума. В частности, это бактерии Achromobacter, Micrococcus, Flavobacterium, Paracoccus и др. Их колонии образуются стадийно. Одни виды вытесняют другие. Помутнение воды в недавно запущенном аквариуме (т.н. "бактериальная муть") является как раз проявлением взрывообразного размножения одних микроорганизмов, чаще - инфузорий, с постепенной заменой их другими и/или падением размера популяции.
Каждая из стадий азотного цикла осуществляется своими бактериями. Аммиак-окисляющие бактерии Nitrosococcus и Nitrosomonas осуществляют процесс NH 3 (NH 4 +) => NO 2 - , а нитрит-окисляющие Nitraspira и Nitrobacter - процесс NO 2 - => NO 3 - .
Процесс заселения аквариума полезными бактериями происходит постепенно. Для успешной работы им требуется определенные условия: пища (аммиак и нитриты), кислород, приемлемая гидрохимия, температура и субстрат, где они будут селиться. Согласно исследованиям оптимальные условия для развития бактерий Nitraspira spp.: концентрация нитритов 0,35 mM, pH 7,6–8,0, температура 39°C. Последнее, естественно, это не означает необходимости разогревать аквариум до столь экстремальной температуры, для большинства аквариумных рыб она является смертельной. Нитрификаторы будут замечательно работать и при 22–28°С. Следует также помнить, что при повышенных значениях температуры и pH возрастает процентное содержание неионизированного аммиака.
Основным местом жительства (субстратом) для аммонифицирующих и нитрифицирующих бактерий являются фильтры, особенно внешние, с внушительным объемом и большой площадью поверхности различных наполнителей. Конечно, эти бактерии живут и в толще воды, но там их значительно меньше. В принципе, в качестве субстрата подходит любая поверхность, но она должна иметь достаточно большую площадь. Голых стенок аквариума для создания работоспособной популяции недостаточно. В аквариумах, лишенных биологического фильтра, в роли субстрата, выступает грунт, однако в нем ощущается дефицит другого жизненно важного компонента нитрификации - кислорода. Поэтому проточный биофильтр является оптимальным для заселения нитрификаторами. См. также статью " ".
Хотя нитрифицирующие бактерии присутствуют повсюду, даже в хлорированной водопроводной воде и в воздухе (отдельные клетки или микроколонии), в свежезапущенном аквариуме их катастрофически мало. Размножаются бактерии быстро - удвоение популяции происходит за 12–32 часа. Однако, согласно исследованиям аквариумов и биофильтров, для налаживания нитрификации требуется от 12 до 22 дней.
Вначале в аквариуме нет нитритов, только аммиак и аммоний, и нарождаются одни аммиак-окисляющие бактерии. По мере появления нитритов в действие включаются нитрит-окисляющие бактерии. Причем есть основания считать, что колония нитрит-окисляющих бактерий прихотливее, рост ее более медленный, и ей может быть причинен больший урон, чем первой колонии при том же воздействии. Например, известно, что Nitraspira могут подавляться даже избытками аммиака. А если учесть, что пищу для их поставляет первая колония, то неудивительно почему задержка в переработке нитритов в новом аквариуме может быть долгой. А потом наоборот исчерпывается аммиак, и аммиак-окисляющие бактерии начинают голодать и сокращать популяцию, зато теперь много пищи для нитрит-окисляющих бактерий... Таким образом, получаются два взаимосвязанных, но разбалансированных цикла со своими пиками и спадами, и задача биофильтрации состоит в том, чтобы эти циклы синхронизировать и развить, и добившись баланса обеих групп бактерий, гибко реагировать на любые изменения аквариумной биохимии.
"Опрокидывание" биофильтра
При неблагоприятных условиях, например, отсутствие питания или достаточного количества кислорода, бактерии переходят в т.н. инактивное состояние ("спячка"), когда минимальный энергетический обмен поддерживается для обеспечения основных функций клетки. При возобновлении подходящих условий бактерия "просыпается". Но если инактивный период длится слишком долго, наступает смерть и распад бактериальной клетки.
Особенно критичны для колоний нитрифицирующих бактерий в биофильтре длительные отключения электричества и сильное загрязнение субстрата с образованием в нем застойных анаэробных зон. Причем опасно не столько само прекращение процесса нитрификации, сколько то, что на их месте поселяются другие, гетеротрофные бактерии, и в анаэробной (безкислородной) среде начинается противоположный процесс - . И при этом велика вероятность, что он пойдет по "неправильным" сценариям - с образованием таких таких ядовитых соединений, как сероводород (H 2 S) и метан (CH 4), или остановится на стадии восстановления нитрата в нитрит. И хорошо, если обойдется просто временным помутнением воды, но может обернуться и массовым замором рыбы. Падение производительности (напора воды) фильтра, как правило, свидетельствует о загрязнении субстрата. Если напор упал ниже 30–40% от максимального, фильтр следует промыть и перезапустить заново, иначе это может привести к его биологическому "опрокидыванию". Не следует также отключать фильтр на продолжительное время. Сильно загрязненный фильтр может представлять опасность для обитателей аквариума уже через 2–3 часа простоя; менее загрязненные могут сравнительно легко пережить без притока свежей воды нескольких часов или даже суток. Кроме степени загрязненности фильтра это зависит от многих факторов, в т.ч. объема аквариума (в больших аквариумах биохимия гораздо более стабильна) и плотности посадки рыб. Но лучше лишний раз этим не рисковать.
"Бактериальная муть"
Под этим термином обычно понимается помутнение или побеление воды, нередко сопровождающееся затхлым запахом. Данное явление характерно для аквариумов с неразвитой или нарушенной биофильтрацией, либо случается от переизбытка органики (при перекорме или при перенаселении). Также может быть вызвано большим вливанием свежей воды или использованием "аквахимии". Еще один "верный" способ получить сильное помутнение воды - налить в аквариум некоторую дозу спирта или водки (но об этом чуть позже). "Бактериальная" или, как ее еще называют "инфузорная" муть является проявлением бурного размножения в аквариумной воде одноклеточных организмов, в большинстве своем гетеротрофных, и их конкуренции между собой. Эти процессы Самвел Купалян метко назвал "междоусобными войнами" микроорганизмов. Сама по себе "бактериальная муть" не опасна для рыб, хотя косвенно является признаком неблагоприятной обстановки в аквариуме и внешне представляет собой малоэстетичное зрелище. Но прямой зависимости между мутностью воды и содержанием вредных веществ в аквариуме нет. Растворенные в воде токсичные соединения азота, возникающие в результате отсутствия или нарушения биофильтрации, незаметны для глаза. Возможна ситуация, когда вода помутнела, а тесты на аммиак и нитрит показывают нулевую или очень низкую концентрацию этих веществ. Но может быть и наоборот: вода в аквариуме кристально прозрачная, а нитриты зашкаливают.
В заново запускаемом аквариуме вода может сильно помутнеть на второй-третий
день (хрестоматийный, но вовсе не обязательный случай). Если система правильно
оборудована и обслуживается, то через несколько дней "бактериальная
муть" исчезает сама собой. Когда помутнение возникает в зрелом аквариуме,
оно проходит после устранения причины его возникновения. И первое, что
я рекомендую сделать, если обнаружилось, что вода "ни с того ни с
сего" помутнела - это усилить аэрацию. В качестве радикального способа
устранения бактериальной мути нередко советуют УФ-стерелизатор. При прохождении
через ультрафиолетовое излучение создающие муть микроорганизмы гибнут,
и вода становится прозрачной. Однако следует понимать, что таким
образом не устраняется первопричина возникновения мути.
Немного истории
Если вы откроете старые книжки, то прочтете там много интересного и правильного о таких химических показателях воды как PH, электропроводимость и жесткость, а также хитроумных способах их измерения, однако не найдете ни слова ни о биофильтрах, ни об азотном цикле. Первого тогда просто не существовало, второе же характеризовалось неким абстрактным понятием "биологическое равновесие", которое наступает само собой через несколько недель после запуска аквариума. Видовой состав рыб - в основном, "живородка" и "харацинка" - и наличие в аквариумах большого числа живых растений в значительной мере компенсировали эти пробелы в теоретических знаниях и технической оснащенности. Думаю, что серьезное отставание нашей страны в области цихлидоводства было в известной мере обусловлено именно этими "особенностями национальной аквариумистики". Ведь содержание цихлид предъявляет к фильтрации повышенные требования. В более поздних публикациях наших авторитетных аквариумистов необходимость аквариумных фильтров признается. " Современная аквариумистика отвечает на этот вопрос положительно",- декларирует Игорь Иванович Ванюшин в опубликованной в 1999 г. в журнале "Миллион Друзей" статье "Нужна ли в аквариуме фильтрация?" Тогда же в литературе появилось множество руководств по изготовлению самодельных внутренних фильтров из пластиковой бутылки и т.п. "Невозможно себе представить, сколько существует конструкций фильтров,- пишет Игорь Иванович,- более того, почти каждый аквариумист вносит свой вклад, изменяя виденное или создавая что-то оригинальное, свое, в ту пору когда всерьез заинтересуется фильтрацией воды".
Одновременно пришло понимание необходимости регулярных подмен воды с целью устранения из нее нитратов и других вредных веществ. То было удивительное время прозрения, когда аквариумистам открылись причины необъяснимых смертей и заболеваний их питомцев. Первые отечественные биофильтры появились еще в 1980-х годах, причем подчас обладали весьма замысловатыми конструкциями. Недостатками самодельных внешних фильтров, которые в значительной мере сводили на нет их достоинства, были громоздкость и ненадежность. Поэтому отношение к внешним фильтрам, даже несмотря на появление в продаже эргономичных и надежных импортных канистровых фильтров, по-прежнему было настороженным. Мнение И.И. Ванюшина (статья "Покупаем Аквариумы" в журнале "Миллион Друзей" №1.2000) на этот счет достаточно показательно: " Не вникая в детали, все фильтры можно разделить на наружные и внутренние. Какой лучше - судите сами, если свою главную задачу по очистке от мусора и вредных примесей они выполняют примерно одинаково... Наружный фильтр почти не ограничивает собой внутреннего пространства аквариума. Внутри проходят только две трубки - для откачивающей и нагнетающей магистралей, все остальное - снаружи. Этим, пожалуй, и ограничиваются его достоинства" . Серьезным противопоказанием против брендовых канистр была их высокая стоимость, а китайские сильно уступали им по качеству. Поэтому многие аквариумисты-любители отдавали предпочтение широко распространившимся у нас в стране в конце 1990-х годов стаканным внутренним фильтрам, сочетающим в себе стильный дизайн и доступную цену, при этом явно преувеличивая их возможности в отношении биофильтрации, а в профессиональной аквариумистике получили распространение встроенные биофильтры. Еще одной альтернативой и своеобразным этапом становления биофильтрационной техники в России был так называемый эрлифт, состоящий из большой губки, подъемной трубы и аэратора. Этот вид фильтра и сейчас успешно используется в выростных аквариумах.
Рассказ Евгения Цигельницкого: "Никогда не забуду свой первый фильтр - разбирающуюся пополам, щелястую коробочку в полстакана из розово-белого "под мрамор" пластика (из такого делали самые дешевые мыльницы) на сизой, скверно пахнущей присоске, жиденько заполненную какими-то нитками, через неделю ставшими совершенно похожими на сопли. К нему сверху через поганенький резиновый переходник крепился простейший эрлифт из пары стеклянных трубок - потолще и потоньше. А набитые в фильтр нитки "сообразительные мы" (с отцом) заменили на мочалку для посуды. Помню и тот фильтр, и мое детское изумление от того, сколько эта маленькая, убогая штуковина за неделю собирала всякой грязи в моем скромном, чистеньком на взгляд трехведерном аквариуме (полностью нагружая собой целый трескучий компрессор). Продвинутые люди тогда пользовали эрлифты из братской ГДР, мне тоже такой привез после долгого нытья дед аж из Ленинграда. И я стал продвинутым – с нереальной, убойной ГДРовской губкой в трехведернике и переехавшей в ведерный ("школьный") малечник мраморной "мыльницей". Целых два фильтра было - во как! Кстати, эта губка у меня трудилась–служила–кочевала по аквариумам почти пятнадцать лет. До сих пор жалею, что она куда-то делась… То есть - воду в аквариумах люди фильтровали еще при советской власти, но большинство фильтрующих – не делало из этого культа, и никоим образом не заботилось происходящими при этом биохимическими событиями… Грязь собрал - и ладно…"
Денитрификация и денитрифицирующие бактерии
Процесс восстановления нитратов до газообразных оксидов и молекулярного азота называется денитрификацией. Это вторая часть азотного цикла. В пресноводной аквариумистике этот процесс используется крайне редко, но тем не менее несомненно заслуживает рассмотрения. В отличие от нитрификации, где важнейшую роль играет растворенный в воде кислород, процессы денитрификации происходят в среде, лишенной кислорода, или, говоря научным языком, анаэробной. Денитрификация определена как превращение нитрата в азот - безвредный газ, который уходит пузырьками наружу. Между начальным продуктом (нитратом) и конечным продуктом (газообразным азотом) существуют три промежуточных продукта: в порядке их возникновения, это нитрит (NO 2), окись азота (NO) и закись азота (N 2 O). То есть денитрификация (как и нитрификация) - это процесс многоступенчатый, и его промежуточные продукты, и в частности нитрит, токсичны. Если денитрификация происходит не до конца, качество воды становится для рыб много хуже, чем до этого процесса. Существуют и еще два других процесса, которые могут происходить в аквариуме. Это диссимилятивное и ассимилятивное поглощение нитрата. Оба они опасны, т.к. производят аммоний. Фактически это полная противоположность нитрификации - нитрат редуцируется в нитрит, который затем редуцируется в гидроксиламин (NH 2 OH) и затем в аммоний.
За все эти превращения ответственны бактерии. Важное различие между нитрификацией и денитрификацией заключается в видах бактерий, которые участвуют в этих процессах. Нитрификация производится так называемыми автотрофными бактериями. Это означает, что они получают углерод, необходимый для роста, из неорганических веществ, в частности, из углекислого газа. Денитрифицирующие бактерии (Bacillus, Denitrobacillas, Micrococcus, Pseudomonas и др.) являются гетеротрофными, то есть получают углерод из органических источников, как сахароза, глюкоза, спирты, органические кислоты, аминокислоты и др. (существует, впрочем, особый вид фильтра-денитратора, в котором для переработки нитрата в азот используется серные бактерии - автотрофы, см. 3-ю часть статьи). Суть полезного действия бактерий-денитрифаторов в том, что в условиях анаэробной, т.е. крайне бедной кислородом среды, они извлекают необходимый для дыхания кислород из нитрата, при этом редуцируя его. Денитрифицирующие бактерии – это анаэробные бактерии. Хотя, если быть совсем корректным, есть бактерии, которые являются факультативными анаэробами и в зависимости от содержания в среде кислорода способны черпать его как из вне, так и извлекать из нитратов (поэтому, кстати, считается, что приспособление денитрифицирующих бактерий к анаэробным условиям - вторичного происхождения). Но в целом, как об этом пишет Мартин Сандер, "можно исходить из того, что кислород препятствует денитрификации".
Таким образом, для успешного протекания процесса денитрификации нужно соблюдение трех условий: наличие в аквариуме нитратов, бедная кислородом среда и наличие органических углеродосодержащих веществ. Углерод используется бактериями как основное питательное средство, в то время как потребность в кислороде удовлетворяется за счет нитрата. Четвертое условие, о котором позже будет рассказано, - это достаточно низкий окислительно-востановительный (или как его обычно называют, редокс) потенциал.
Реакцию денитрификации в классическом ее виде можно выразить уравнениями:
первая ступень 3NO 3 - + CH 3 OH = 3NO 2 - + CO 2 + 2H 2 O и
вторая ступень 2NO 2 - + CH 3 OH = N 2 + CO 2 + H 2 O + 2OH - .
Как видно из уравнений, нитраты при этом не сразу трансформируются в газообразный азот, а прежде образуются токсичные нитриты. И лишь на второй ступени азот удаляется из цикла путем образования газообразного азота. Добиться, чтобы эти процессы происходили контролируемо, - непростая задача. Во всяком случае, это гораздо сложнее, чем наладить биологическое преобразование аммиака в нитрат. Кроме того, с денитрификацией связано немало заблуждений, в том числе исходящих от аквариумистистов, использующих эти технологии на практике. Процесс денитрификации не всегда происходит безмятежно. Наряду с полезным действием по удалению нитратов, в ходе денитрификационных процессов могут образовываться другие вещества, чрезвычайно вредные - метан (СН 4) и сероводород (H 2 S), поскольку наряду денитрифицирующими бактериями в анаэробные процессы подключаются и другие виды микроорганизмов, в частности метанобразующие археи и сульфатвосстанавливающие бактерии, тоже анаэробы. В частности, такое происходит, при недостатке нитратов, либо очень низком редокс-потенциале. Тогда анаэробная микрофлора начинает удовлетворять потребность в кислороде за счет других кислородосодержащих химических соединений - с выделением сероводорода и метана, оба газа токсичны. Метанобразующие бактерии могут синтезировать метан, используя в качестве энергии реакции окисления углекислого газа (СО 2). В природных водоемах метан является одним из конечных продуктов разложения органических веществ в донной анаэробной зоне и образуется узкоспециализированной группой строгих анаэробов - метанобразующих архей. Сульфатвосстанавливающие бактерии забирают кислород из сульфатов (SO 4 2-). В этом процессе, который называется десульфуризация, возникает сероводород, который известен запахом тухлых яиц. Также выше упомянуты биопроцессы диссимилятивного и ассимилятивного восстановления нитратов до гидроксиламина (NH 2 OH) и затем аммония. Способностью к этому обладают различные бактерии, а также некоторые актиномицеты и грибы. Понятно, что всеми этими процессами, которые также происходят в природе, трудно управлять в аквариуме, стимулируя лишь полезные и препятствуя вредным процессам.
Теперь несколько слов об окислительно-восстановительном потенциале - мере способности химического вещества присоединять электроны (восстанавливаться). Его величина определяет равновесие между восстановительными и окислительными реакциями в воде. Другое название - редокс-потенциал (от англ. redox - reduction-oxidation reaction). Этот показатель связан с уровнем загрязненности аквариумной воды органическими веществами, а также с возрастом аквариума. Недавно запущенный аквариум характеризуется, как правило, высокими значениями редокс потенциала, затем, по мере старения аквариума, его редокс-потенциал снижается. Поддерживать редокс-потенциал на определенном уровне можно путем регулярного ухода за аквариумом, чистки грунта, подмены воды и т.д. Высокий положительный редокс-потенциал (в нормальном аквариуме он составляет 200 – 400 mV (минивольт)) указывает на доминирование окислительных реакций над восстановительными. Отрицательный редокс потенциал указывает на отсутствие кислорода в воде, что смертельно для большинства беспозвоночных. А вот для нормального течения процесса денитрификации окислительно-восстановительный потенциал должен быть отрицательным и удерживаться в пределах примерно от -50 до -250 mV. Таким образом, реакция денитрификации не может происходить непосредственно аквариумной воде, а требует специальных анаэробных зон, которые могут образовываться, например, в грунте или фильтре. Если же окислительно-восстановительный потенциал будет выше, чем -50 mV (но меньше нуля), то процесс денитрификации скорее всего остановится на стадии образования нитритов. А если он упадет ниже -300 mV, то бактерии возьмутся за сульфаты.
Следующая проблема - наличие достаточного количества органического углерода, необходимого для этого виды бактерий. Органических веществ, находящихся в аквариуме, не достаточно для поддержки процесса, поэтому требуется вносить их дополнительно. В выше приведенных уравнениях в качестве органического вещества фигурирует метанол, однако на практике метиловый спирт - яд. Концепция классического углеродного нитратредуктора подразумевает использование лактозы. Еще вариант - этиловый спирт или водка. Кстати, несколько лет назад очень популярной была идея запуска денитрификации посредством внесения в аквариум водки. Правда, отваживались на это не многие, но обсуждали активно. На самом деле, как пишет об этом Дитер Брокманн, эта технология не имеет ничего общего с денитрификацией, то есть расщеплением нитратов для дыхания бактерий, а скорее ближе к ассимиляции и производству биомассы. "Алкоголем, в отличие от денитрифицирующих фильтров, мы стимулируем преимущественно аэробных бактерий и только затем анаэробных бактерий, играющих менее важную роль. Под ассимиляцией подразумевается усвоение нитратов и фосфатов, например, водорослями. Последние используют оба вещества для получения азота и фосфора, необходимых для собственного обмена веществ и, соответственно, жизнеобеспечения и роста. Из этого следует вывод, что усиленный рост водорослей влияет на понижение концентрации фосфатов и нитратов в аквариуме. Раньше этот эффект использовали в водорослевых фильтрах для редукции нитратов. Подливая водку в аквариум, мы тем самым поддерживаем ассимиляцию, стимулируя, правда, не водоросли, а бактерии. Мы предоставляем им источник легко перерабатываемой пищи - этанол в водке. За счет наращивания биомассы уровень содержания фосфатов и нитратов в аквариумной воде снижается. Однако практика показала, что денитрификация может протекать только в субстрате, содержащем анаэробные зоны. И о его наличии тоже надо позаботиться".
И еще. Нужно сбалансировать систему так, чтобы промежуточные продукты денитрификации не накапливались. Как выше указывалось, при переработке нитрата сначала производится нитрит, он токсичен и накапливаться в аквариуме не должен. Опасность роста концентрации нитрита - одно из слабых мест денитрифицирующих систем. Ну и чтобы совсем сгустить краски, надо напомнить, что кроме нитратов в аквариуме еще есть фосфаты и наверное еще много разных веществ и соединений, которые нельзя проконтролировать с помощью стандартного набора аквариумных тестов, из-за чего дискусы в зацикленном с помощью денитратора аквариуме вдруг становятся вялыми и отказываются нереститься. Селективным устранением нитратов мы добиваемся только видимости создания системы замкнутого цикла.
Впрочем все это не означает, что денитрификация, в принципе, недоступна или не имеет смысла для аквариумистики. Нитратные фильтры уже много лет успешно используются в морских аквариумах и сейчас начали внедряться для обслуживания в пресноводных. Но более всего хочется надеяться, что денитрификация все еще представляет собой перспективную область для исследований, и последнее слово в этом вопросе еще не сказано.
Литература
Аникштейн С. Нитраты – такие вредные и такие полезные.
Аникштейн С. Не пренебрегайте аэрацией.
Бейли М. Бергесс П. Золотая книга аквариумиста.
Берсенев А. Загадка биофильтра.
Брокман Д. Нитраты.
Ванюшин И.И. Нужна ли в аквариуме фильтрация?
Ванюшин И.И. Покупаем аквариумы.
Горюшкин С. Обратный осмос в системе фильтрации аквариума.
Горюшкин С. Фильтрация и дискусы.
Гусев М.В., Минеева Л.А. Микробиология.
Дубиновский М. и др. Вода в аквариуме.
Дубиновский М. и др. Фильтрация в аквариуме.
Дубиновский М. Запуск аквариума.
Информационные материалы по морской аквариумистике, разные.
Кубасов А.А. Цеолиты – кипящие камни.
Ковалев В. В аквариуме что-то не так??? Попробуем разобраться!
Ковалев В. Пять очень важных параметров качества воды и как ими пользоваться
не запутавшись.
Ковалев В. Состав аквариумной воды: основные проблемы.
Кусков В. Как создавать и поддерживать биологическое равновесие.
Сандер М. Техническое оснащение аквариума.
Серга Т. Nitrospira – нитрит-окисляющие бактерии в аквариумах.
Спиридонов М. Цеолит в аквариуме. Польза или вред?
Телегин А. Устройство открытых фильтров.
Успех с нитратным фильтром. Пер. А.И. Горюшкина.
Фролов Ю., Юдаков В. Основы биологической фильтрации.
Хахинов В.В. и др. Гидрохимия экстремальных водных систем с основами гидробиологии.
Хованек Т. Что такое денитрификация?
Хомченко И.Г. и др. Современный аквариум и химия.
Цигельницкий Е. Фитофильтрация.
Шереметьев И. Орошаемый фильтр для аквариума.
Элбакян В. Жуть нитратная.
Юдаков В. Краткие основы аквариумной фильтрации.
Ярцев В. Заметки по поводу биошаров (Bioballs).
Ярцев В. Фильтры с орошением (sump).
Brockmann D. Fische und Korallen im Meer und im Aquarium.
Holmes-Farley R. Chemistry and the aquarium: Nitrate in the reef aquarium.
Foster С. Exclusive: Hagen announces launch of Fluval G filter.
© Е. Грановский, 2009-2010
Еще в 1870 г. Шлезинг и Мюнц (Schloesing, Miintz) доказали, что нитрификация имеет биологическую природу. Для этого они добавляли к сточным водам хлороформ. В результате окисление аммиака прекращалось. Однако специфические микроорганизмы, вызывающие этот процесс, были выделены лишь Виноградским. Им же было показано, что хемоавтотрофные нитрификаторы могут быть подразделены на бактерий, осуществляющих первую фазу этого процесса, а именно окисление аммония до азотистой кислоты (NH4+->N02-), и бактерий второй фазы нитрификации, переводящих азотистую кислоту в азотную (N02-->-N03-). И те и другие микроорганизмы являются грамотрицательными. Их относят к семейству Nitrobacteriaceae.
Бактерии первой фазы нитрификации представлены четырьмя родами: Nitrosomonas, Nitrosocystis, Nitrosolobus и Nitrosospira. Из них наиболее изучен вид Nitrosomonas euroраеа, хотя получение чистых культур этих микроорганизмов, как и других нитрифицирующих хемоавтотрофов, до сих пор остается достаточно сложным. Клетки N. europaea обычно овальные (0,6 -1,0 X 0,9-2,0 мкм), размножаются бинарным делением. В процессе развития культур в жидкой среде наблюдаются подвижные формы, имеющие один или несколько жгутиков, и неподвижные зооглеи.
У Nitrosocystis oceanus клетки округлые, диаметром 1,8-2,2 мкм, но бывают и крупнее (до 10 мкм). Способны к движению благодаря наличию одного жгутика или пучка жгутиков. Образуют зооглеи и цисты.
Размеры Nitrosolobus multiformis составляют 1,0-1,5 X 1,0-2,5 мкм. Форма этих бактерий не совсем правильная, так как клетки разделены на отсеки, дольки (-lobus, отсюда и название Nitrosolobus), которые образуются в результате разрастания внутрь цитоплазматической мембраны.
У Nitrosospira briensis клетки палочковидные и извитые (0,8-1,0 X 1,5-2,5 мкм), имеют от одного до шести жгутиков.
Среди бактерий второй фазы нитрификации различают три рода: Nitrobacter, Nitrospina и Nitrococcus.
Большая часть исследований проведена с разными штаммами Nitrobacter, многие из которых могут быть отнесены- к Nitrobacter winogradskyi, хотя описаны и другие виды. Бактерии имеют преимущественно грушевидную форму клеток. Как показано Г. А. Заварзиным, размножение Nitrobacter происходит путем почкования, причем дочерняя клетка бывает обычно подвижна, так как снабжена одним латерально расположенным жгутиком. Отмечают также сходство Nitrobacter с почкующимися бактериями рода Hyphomicrobium по составу жирных кислот, входящих в липиды.
Данные относительно таких нитрифицирующих бактерий, как Nitrospina gracilis и Nitrococcus mobilis, пока весьма ограниченны. По имеющимся описаниям, клетки N. gracilis палочковидные (0,3-0,4 X 2,7-6,5 мкм), но обнаружены и сферические формы. Бактерии неподвижны. Напротив, N. mobilis обладает подвижностью. Клетки его округлые, диаметром около 1,5 мкм, с одним-двумя жгутиками.
По строению клеток исследованные нитрифицирующие бактерии похожи на другие грамотрицательные микроорганизмы. У некоторых видов обнаружены развитые системы внутренних мембран, которые образуют стопку в центре клетки (Nitrosocystis oceanus), или располагаются по периферии параллельно цитоплазматической мембране (Nitrosomonas europaea), или образуют чашеподобную структуру из нескольких слоев (Nitrobacter winogradskyi). Видимо, с этими образованиями связаны ферменты, участвующие в окислении нитрификаторами специфических субстратов.
Нитрифицирующие бактерии растут на простых минеральных средах, содержащих окисляемый субстрат в виде аммония или нитритов и углекислоту. Источником азота в конструктивных процессах могут быть, кроме аммония, гидроксиламин и нитриты.
Показано также, что Nitrobacter и Nitrosomonas europaea восстанавливают нитриты с образованием аммония.
Такой микроорганизм, как Nitrosocystis oceanus, выделенный из Атлантического океана, относится к облигатным галофилам и растет на среде, содержащей морскую воду. Область значений рН, при которой наблюдается рост разных видов и штаммов нитрифицирующих бактерий, приходится на 6,0-8,6, а оптимальное значение рН чаще всего 7,0-7,5. Среди Nitrosomonas europaea известны штаммы, имеющие температурный оптимум при 26 или около 40 °С, и штаммы, довольно быстро растущие при 4 °С.
Все известные нитрифицирующие бактерии являются облигатными аэробами. Кислород необходим им как для окисления аммония в азотистую кислоту:
так и для окисления азотистой кислоты в азотную:
Но весь процесс превращения аммония в нитраты происходит в несколько этапов с образованием соединений, где азот имеет разную степень окисленности.
Первым продуктом окисления аммония является гидроксиламин, который, возможно, образуется в результате непосредственного включения в NH+4 молекулярного кислорода:
Однако окончательно механизм окисления аммония до гидроксиламина не выяснен. Превращение гидроксиламина в нитрит:
как предполагают, идет через образование гипонитрита NOH, а также окись азота (NO). Что касается закиси азота (N2O), обнаруживаемой при окислении Nitrosomonas europaea аммония и гидроксиламина, то большинство исследователей считает ее побочным продуктом, образующимся в основном в результате восстановления нитрита.
Исследование окисления Nitrobacter нитрита с использованием в опытах тяжелого изотопа кислорода (18O) показало, что образующиеся нитраты содержат значительно больше 18O, когда меченой является вода, а не молекулярный кислород. Поэтому предполагают, что сначала происходит образование комплекса NO2-H2O, который далее окисляется до NO2-. При этом происходит передача электронов через промежуточные акцепторы на кислород. Весь процесс нитрификации можно представить в виде следующей схемы (рис. 137), отдельные этапы которой требуют, однако, уточнения.

Кроме первой реакции, а именно образования из аммония гидроксиламина, последующие стадии обеспечивают организмы энергией в виде аденозинтрифосфата (АТФ). Синтез АТФ сопряжен с функционированием окислительновосстановительных систем, передающих электроны на кислород, подобно тому как это имеет место у гетеротрофных аэробных организмов. Но поскольку окисляемые нитрификаторами субстраты имеют высокие окислительно-восстановительные потенциалы, они не могут взаимодействовать с никотинамидадениндинуклеотидами (НАД или НАДФ, E1/0 = -0,320 В), какэто бывает при окислении большинства органических соединений. Так, передача электронов в дыхательную цепь от гидроксиламина, видимо, происходит на уровне флавина:
Когда окисляется нитрит, то включение его электронов в цепь, вероятно, идет на уровне либо цитохрома типа с, либо цитохрома типа а. В связи с этой особенностью большое значение у нитрифицирующих бактерий имеет так называемый обратный, или обращенный, транспорт электронов, идущий с затратой энергии части АТФ или трансмембрапного потенциала, образуемых при передаче электронов на кислород (рис. 138).

Таким образом происходит обеспечение хемоавтотрофных нитрифицирующих бактерий не только АТФ, но и НАДН, необходимых для усвоения углекислоты и для других конструктивных процессов.
Согласно расчетам эффективность использования свободной энергии Nitrobacter может составлять 6,0-50,0%, a Nitrosomonas - и больше.
Ассимиляция углекислоты происходит в основном в результате функционирования пентоэофосфатного восстановительного цикла углерода, иначе называемого циклом Кальвина (см. рис. 134).

Итог его выражают следующим уравнением:
где (СН2О) означает образующиеся органические вещества, имеющие уровень восстановленности углеродов. Однако в действительности в результате ассимиляции углекислоты через цикл Кальвина и другие реакции, прежде всего путем карбоксилирования фосфоенолпирувата, образуются не только углеводы, но и все другие компоненты клеток - белки, нуклеиновые кислоты, липиды и т. д. Показано также, что Nitrococcus mobilis и Nitrobacter winogradskyi могут образовывать в качестве запасных продуктов поли-β-оксибутират и гликогеноподобный полисахарид. Такое же соединение обнаружено в клетках Nitrosolobus multiformis. Кроме углеродсодержащих запасных веществ, нитрифицирующие бактерии способны накапливать полифосфаты, входящие в состав метахроматиновых гранул.
Еще в первых работах с нитрификатором Виноградский отметил, что для их роста неблагоприятно присутствие в среде органических веществ, таких, как пептон, глюкоза, мочевина, глицерин и др. Отрицательное действие органических веществ на хемоавтотрофные нитрифицирующие бактерии неоднократно отмечалось и в дальнейшем. Сложилось даже мнение, что эти микроорганизмы вообще не способны использовать экзогенные органические соединения. Поэтому их стали называть «облигатными автотрофами». Однако в последнее время показано, что использовать некоторые органические соединения эти бактерии способны, но возможности их ограничены. Так, отмечено стимулирующее действие на рост Nitrobacter в присутствии нитрита дрожжевого автолизата, пиридоксина, глутамата и серина, если они в низкой концентрации вносятся в среду. Показано также включение в белки и другие компоненты клеток Nitrobacter 14С из пирувата, а-кетоглутарата, глутамата и аспартата. Известно, кроме того, что Nitrobacter медленно, но окисляет формиат. Включение 14С из ацетата, пирувата, сукцината и некоторых аминокислот, преимущественно в белковую фракцию, обнаружено при добавлении этих субстратов к суспензиям клеток Nitrosomonas europaea. Ограниченная ассимиляция глюкозы, пирувата, глутамата и аланина установлена для Nitrosocystis oceanus. Есть данные об использовании 14С-ацетата Nitrosolobus multiformis.
Недавно установлено также, что некоторые штаммы Nitrobacter растут на среде с ацетатом и дрожжевым автолизатом не только в присутствии, но и в отсутствие нитрита, хотя и медленно. При наличии нитрита окисление ацетата подавляется, но включение его углерода в разные аминокислоты, белок и другие компоненты клеток увеличивается. Имеются, наконец, данные, что возможен рост Nitrosomonas и Nitrobacter на среде с глюкозой в анализируемых условиях, которые обеспечивают удаление продуктов ее метаболизма, оказывающих ингибиторное действие на данные микроорганизмы. На основании этого делается вывод о способности нитрифицирующих бактерий переключаться на гетеротрофный образ жизни. Однако для окончательных выводов необходимо большее число экспериментов. Важно прежде всего выяснить, как долго нитрифицирующие бакте рии могут расти в гетеротрофных условиях при отсутствии специфических окисляемых субстратов.
Хемоавтотрофные нитрифицирующие бактерии имеют широкое распространение в природе и встречаются как в почве, так и в разных водоемах. Осуществляемые ими процессы могут происходить весьма в крупных масштабах и имеют существенное значение в круговороте азота в природе. Раньше считали, что деятельность нитрификаторов всегда способствует плодородию почвы, поскольку они переводят аммоний в нитраты, которые легко усваиваются растениями, а также повышают растворимость некоторых минералов. Сейчас, однако, взгляды на значение нитрификации несколько изменились. Во-первых, показано, что растения усваивают аммонийный азот и ионы аммония лучше удерживаются в почве, чем нитраты. Во-вторых, образование нитратов иногда приводит к нежелательному подкислению среды. В-третьих, нитраты могут восстанавливаться в результате денитрификации до N2, что приводит к обеднению почвы азотом.
Следует также отметить, что наряду с нитрифицирующими хемоавтотрофными бактериями известны гетеротрофные микроорганизмы, способные вести близкие процессы. К гетеротрофным нитрификаторам относятся некоторые грибы из рода Fusarium и бактерии таких родов, как Alcaligenes, Corynebacterium, Achromobacter, Pseudomonas, Arthrobacter, Nocardia.
Показано, что Arthrobacter sp. окисляет в присутствии органических субстратов аммоний с образованием гидроксиламина и далее нитритов и нитратов. Кроме того, может образовываться гидроксамовая кислота. У ряда бактерий выявлена способность осуществлять нитрификацию органических азотсодержащих соединений: амидов, аминов, оксимов, гидроксаматов, нитросоединений и др. Пути их превращения представляют следующим образом:

Размеры гетеротрофной нитрификации в некоторых случаях бывают довольно большие. Кроме того, при этом образуются некоторые продукты, обладающие токсичным, канцерогенным, мутагенным действием и соединения с химиотерапевтическим эффектом. Поэтому исследованию данного процесса и выяснению его значения для гетеротрофных микроорганизмов сейчас уделяют значительное внимание.
Жизнь растений: в 6-ти томах. - М.: Просвещение. Под редакцией А. Л. Тахтаджяна, главный редактор чл.-кор. АН СССР, проф. А.А. Федоров . 1974 .
Превращают аммиак и аммонийные соли в соли азотной кислоты нитраты: нитрозобактерии, нитробактерии. Распространены в почвах и водоемах … Большой Энциклопедический словарь
Превращают аммиак и аммонийные соли в соли азотной кислоты нитраты: нитрозобактерии, нитробактерии. Распространены в почвах и водоёмах. * * * НИТРИФИЦИРУЮЩИЕ БАКТЕРИИ НИТРИФИЦИРУЮЩИЕ БАКТЕРИИ, превращают аммиак и аммонийные соли в соли азотной… … Энциклопедический словарь
нитрифицирующие бактерии - nitrifikatoriai statusas T sritis ekologija ir aplinkotyra apibrėžtis Nitritinės (Nitrosomonas genties) ir nitratinės (Nitrobacter genties) bakterijos, paverčiančios amonio druskas nitratais. atitikmenys: angl. nitrifiers; nitrifying bacteria vok … Ekologijos terminų aiškinamasis žodynas - проводят реакции окисления восстановленных соединений азота. Представители рода Nitrosomonas окисляют аммиак до нитритов, а бактерии рода Nitrobacter окисляют нитриты до нитратов. Относятся к автотрофным хемосинтезирутощим аэробным… … Геологическая энциклопедия
По типу питания все организмы делятся на автотрофов и гетеротрофов. Автотрофы, что в переводе с греческого означает «самопитающиеся», могут строить все соединения своих клеток из углекислоты и других неорганических веществ. Источником… … Биологическая энциклопедия
Еще в 1870 г. Шлезинг и Мюнц (Schloesing, Muntz) доказали, что нитрификация имеет биологическую природу. Для этого они добавляли к сточным водам хлороформ. В результате окисление аммиака прекращалось. Однако специфические микроорганизмы, вызывающие этот процесс, были выделены лишь Виноградским. Им же было показано, что хемо-автотрофные нитрификаторы могут быть подразделены на бактерий, осуществляющих первую фазу этого процесса, а именно окисление аммония до азотистой кислоты (NH4 + ->NO2 -), и бактерий второй фазы нитрификации," переводящих азотистую кислоту в азотную (N02 - ->NO3 -). И те и другие микроорганизмы являются грамотрицательными. Их относят к семейству Nitrobacteriaceae.
Бактерии первой фазы нитрификации представлены четырьмя родами: Nitrosomonas, Nitrosocystis, Nitrosolobus и Nitrosospira. Из них наиболее изучен вид Nitrosomonas euro-раеа, хотя получение чистых культур этих микроорганизмов, как и других нитрифицирующих хемоавтотрофов, до сих пор остается достаточно сложным. Клетки N. еurораеа обычно овальные (0,6-1,0)< 0,9-2,0 мкм), размножаются бинарным делением. В процессе развития культур в жидкой среде наблюдаются подвижные формы, имеющие один или несколько жгутиков, и неподвижные зооглеи.
У Nitrosocystis oceanus клетки округлые, диаметром 1,8-2,2 мкм, но бывают и крупнее (до 10 мкм). Способны к движению благодаря наличию одного жгутика или пучка жгутиков. Образуют зооглеи и цисты.
Размеры Nitrosolobus multiformis составляют 1,0-1,5 X 1,0-2,5 мкм. Форма этих бактерий не совсем правильная, так как клетки разделены на отсеки, дольки (-lobus, отсюда и название Nitrosolobus), которые образуются в результате разрастания внутрь цитоплазматической мембраны.
У Nitrosospira briensis клетки палочковидные и извитые (0,8 -1,0 X 1,5-2,5 мкм), имеют от одного до шести жгутиков.
Среди бактерий второй фазы нитрификации различают три рода: Nitrobacter, Nitrospina и Nitrococcus.
Большая часть исследований проведена с разными штаммами Nitrobacter, многие из которых могут быть отнесены к Nitrobacter wino-gradskyi, хотя описаны и другие виды. Бактерии имеют преимущественно грушевидную форму клеток. Как показано Г. А. Заварзиным, размножение Nitrobacter происходит путем почкования, причем дочерняя клетка бывает обычно подвижна, так как снабжена одним латерально расположенным жгутиком. Отмечают также сходство Nitrobacter с почкующимися бактериями рода Hyphomicrobium по составу жирных кислот, входящих в липиды.
Данные относительно таких нитрифицирующих бактерий, как Nitrospina gracilis и Nitrococcus mobilis, пока весьма ограниченны. По имеющимся описаниям, клетки N. gracilis палочковидные (0,3-0,4 X 2,7-6,5 мкм), но обнаружены и сферические формы. Бактеррга неподвижны. Напротив, N. mobilis обладает подвижностью. Клетки его округлые, диаметром около 1,5 мкм, с одним-двумя жгутиками.
По строению клеток исследованные нитрифицирующие бактерии похожи на другие грамотрицательные микроорганизмы. У некоторых видов обнаружены развитые системы внутренних мембран, которые образуют стопку в центре клетки (Nitrosocystis oceanus), или располагаются по периферии параллельно цитоплазматической мембране (Nitrosomonas еигораеа), или образуют чашеподобную структуру из нескольких слоев (Nitrobacter winogradskyi). Видимо, с этими образованиями связаны ферменты, участвующие в окислении нитрификаторами специфических субстратов.
Нитрифицирующие бактерии растут на простых минеральных средах, содержащих окисляемый субстрат в виде аммония или нитритов и углекислоту. Источником азота в конструктивных процессах могут быть, кроме аммония, гидроксиламин и нитриты.
Показано также, что Nitrobacter и Nitrosomonas еигораеа восстанавливают нитриты с образованием аммония.
Такой микроорганизм, как Nitrosocystis oceanus, выделенный из Атлантического океана, относится к облигатным галофилам и растет на среде, содержащей морскую воду. Область значений рН, при которой наблюдается рост разных видов и штаммов нитрифицирующих бактерий, приходится на 6,0-8,6, а оптимальное значение рН чаще всего 7,0-7,5. Среди Nitrosomonas еигораеа известны штаммы, имеющие температурный оптимум при 26 или около 40 °С, и штаммы, довольно быстро растущие при 4°С.
Все известные нитрифицирующие бактерии являются облигатными аэробами. Кислород необходим им как для окисления аммония в азотистую кислоту:
NH4 + +3/2O2 ->N02 - + H20+2H + , дельта F = - 27,6.104d;w:,
так и для окисления азотистой кислоты в азотную:
NO2 - +1/2О2 - NO3 - , дельта F = -7,6*104дж.
Но весь процесс превращения аммония в нитраты происходит в несколько этапов с образованием соединений, где азот имеет разную степень окисленности.
Первым продуктом окисления аммония является гидроксиламин, который, возможно, образуется в результате непосредственного включения в NH4 + молекулярного кислорода:
NH4 + +1/2 O2 -> NH2OH+H + , дельта F = + 15,9*103дж.
Однако окончательно механизм окисления аммония до гидроксиламина не выяснен. Превращение гидроксиламина в нитрит:
NH2OH+O2 -> N02 - + H20+H + , дельта F = - 28,9 104 Дж
как предполагают, идет через образование гипонитрита NOH, а также окись азота (N0). Что касается закиси азота (N20), обнаруживаемой при окислении Nitrosomonas europaea аммония и гидроксиламина, то большинство исследователей считает ее побочным продуктом, образующимся в основном в результате восстановления нитрита.
Исследование окисления Nitrobacter нитрита с использованием в опытах тяжелого изотопа кислорода (18 0) показало, что образующиеся нитраты содержат значительно больше 18 0, когда меченой является вода, а не молекулярный кислород. Поэтому предполагают, что сначала происходит образование комплекса N02~H2O, который далее окисляется до N0s~. При этом происходит передача электронов через промежуточные акцепторы на кислород. Весь процесс нитрификации можно представить в виде следующей схемы (рис. 137), отдельные этапы которой требуют, однако, уточнения.
Рис. 131. Структурные формулы некоторых каротиноидов фототрофных бактерий.
Кроме первой реакции, а именно образования из аммония гидроксиламина, последующие стадии обеспечивают организмы энергией в виде аденозинтрифосфата (АТФ). Синтез АТФ сопряжен с функционированием окислительно-восстановительных систем, передающих электроны на кислород, подобно тому как это имеет место у гетеротрофных аэробных организмов. Но поскольку окисляемые нитрификаторами субстраты имеют высокие окислительно-восстановительные потенциалы, они не могут взаимодействовать с никотинамидадениндинуклеотида-ми (НАД или НАДФ, E = -0,320 В), как это бывает при окислении большинства органических соединений. Так, передача электронов в дыхательную цепь от гидроксиламина, видимо, происходит на уровне флавина:
NH2OH -> флавопротеид -> цит. b (убихинон?) ->-> цит. с -> цит. а -> - 02
Когда окисляется нитрит, то включение его электронов в цепь, вероятно, идет на уровне либо цитохрома типа с, либо цитохрома типа а. В связи с этой особенностью большое значение у нитрифицирующих бактерий имеет так называемый обратный, или обращенный, транспорт электронов, идущий с затратой энергии части АТФ или трансмембранного потенциала, образуемых при передаче электронов на кислород (рис. 138).
Рис. 132. Схема переноса электронов при фотосинтезе у растений: П, и П2 - пигменты фотоактивных центров; Z, и Z2 - первичные акцепторы электрона; Фд - ферредоксин; НАДФ - никотинамидадениндинуклеотидфосфат; АТФ - аденозинтрифосфат.
Таким образом происходит обеспечение хемо-автотрофных нитрифицирующих бактерий не только АТФ, но и НАДН, необходимых для усвоения углекислоты и для других конструктивных процессов.
Согласно расчетам эффективность использования свободной энергии Nitrobacter может составлять 6,0-50,0%, a Nitrosomonas - и больше.
Ассимиляция углекислоты происходит в основном в результате функционирования пенто-зофосфатного восстановительного цикла углерода, иначе называемого циклом Кальвина (см. рис. 134). Итог его выражают следующим уравнением:
6С02+18АТФ+12НАДН+12Н + -> -> 6[СН20] + 18АДФ+18Фн+12НАД+6Н20,
где [СН2О] означает образующиеся органические вещества, имеющие уровень восстановлен-ности углеродов. Однако в действительности в результате ассимиляции углекислоты через цикл Кальвина и другие реакции, прежде всего путем карбоксилирования фосфоенолпирувата, образуются не только углеводы, но и все другие компоненты клеток - белки, нуклеиновые кислоты, липиды и т. д. Показано также, что Nitrococcus mobilis и Nitrobacter winogradskyi могут образовывать в качестве запасных продуктов поли-бета-оксибутират и гликогеноподобный полисахарид. Такое же соединение обнаружено в клетках Nitrosolobus multiformis. Кроме углеродсодержащих запасных веществ, нитрифицирующие бактерии способны накапливать полифосфаты, входящие в состав мета-хроматиновых гранул.
Еще в первых работах с нитрификатором Ви-ноградский отметил, что для их роста неблагоприятно присутствие в среде органических веществ, таких, как пептон, глюкоза, мочевина, глицерин и др. Отрицательное действие органических веществ на хемоавтотрофные нитрифицирующие бактерии неоднократно отмечалось и в дальнейшем. Сложилось даже мнение, что эти микроорганизмы вообще не способны использовать экзогенные органические соединения. Поэтому их стали называть «облигатными автотрофами». Однако в последнее время показано, что использовать некоторые органические соединения эти бактерии способны, но возможности их ограничены. Так, отмечено стимулирующее действие на рост Nitro-bacter в присутствии нитрита дрожжевого авто-лизата, пиридоксина, глутамата и серина, если они в низкой концентрации вносятся в среду. Показано также включение в белки и другие компоненты клеток Nitrobacter 14 C из пирувата, альфа-кетоглутарата, глутамата и аспартата. Известно, кроме того, что Nitrobacter медленно, по окисляет формиат. Включение 14 С из ацетата, пирувата, сукцината и некоторых аминокислот, преимущественно в белковую фракцию, обнаружено при добавлении этих субстратов к суспензиям клеток Nitrosomonas europaea. Ограниченная ассимиляция глюкозы, пирувата, глутамата и аланина установлена для Nitrosocystis oceanus. Есть данные об использовании 14 С-ацетата Nitrosolobus multiformis.
Недавно установлено также, что некоторые штаммы Nitrobacter растут на среде с ацетатом и дрожжевым автолизатом не только в присутствии, но и в отсутствие нитрита, хотя и медленно. При наличии нитрита окисление ацетата подавляется, но включение его углерода в разные аминокислоты, белок и другие компоненты клеток увеличивается. Имеются, наконец, данные, что возможен рост Nitrosomonas и Nitrobacter на среде с глюкозой в диализируе-мых условиях, которые обеспечивают удаление продуктов ее метаболизма, оказывающих инги-биторное действие на данные микроорганизмы. На основании этого делается вывод о способности нитрифицирующих бактерий переключаться на гетеротрофный образ жизни. Однако для окончательных выводов необходимо большее число экспериментов. Важно прежде всего выяснить, как долго нитрифицирующие бактерии могут расти в гетеротрофных условиях при отсутствии специфических окисляемых субстратов.
Хемоавтотрофные нитрифицирующие бактерии имеют широкое распространение в природе и встречаются как в почве, так и в разных водоемах. Осуществляемые ими процессы могут происходить весьма в крупных масштабах и имеют существенное значение в круговороте азота в природе. Раньше считали, что деятельность нитрификаторов всегда способствует плодородию почвы, поскольку они переводят аммоний в нитраты, которые легко усваиваются растениями, а также повышают растворимость некоторых минералов. Сейчас, однако, взгляды на значение нитрификации несколько изменились. Во-первых, показано, что растения усваивают аммонийный азот и ионы аммония лучше удерживаются в почве, чем нитраты. Во-вторых, образование нитратов иногда приводит к нежелательному подкислению среды. В-третьих, нитраты могут восстанавливаться в результате денитрификации до N2, что приводит к обеднению почвы азотом.
Следует также отметить, что наряду с нитрифицирующими хемоавтотрофными бактериями известны гетеротрофные микроорганизмы, способные вести близкие процессы. К гетеротрофным нитрификаторам относятся некоторые грибы из рода Fusarmm и бактерии таких родов, как Alcaligenes, Corynebacterium, Achromoba-cter, Pseudomonas, Arthrobacter, Nocardia.
Показано, что Arthrobacter sp. окисляет в присутствии органических субстратов аммоний с образованием гидроксиламина и далее нитритов и нитратов. Кроме того, может образовываться гидроксамовая кислота. У ряда бактерий выявлена способность осуществлять нитрификацию органических азотсодержащих соединений: амидов, аминов, оксимов, гидро-ксаматов, нитросоединений и др. Пути их превращения представляют следующим образом:
Размеры гетеротрофной нитрификации в некоторых случаях бывают довольно большие. Кроме того, при этом образуются некоторые продукты, обладающие токсичным, канцерогенным, мутагенным действием и соединения с хи-миотерапевтическим эффектом. Поэтому исследованию данного процесса и выяснению его значения для гетеротрофных микроорганизмов сейчас уделяют значительное внимание.
22 апреля 2016По типу питания все известные живые организмы делятся на два больших вида: гетеро- и автотрофы. Отличительной особенностью последних является их способность к самостоятельному построению новых элементов из углекислоты и других неорганических веществ.
Источники энергии, поддерживающие их жизнедеятельность, обусловливают их деление на фотоафтотрофы (источник - свет) и хемоавтотрофы (источник - минеральные вещества). А в зависимости от названия субстрата, который окисляют хемоавтортофы, они разделяются на водородные и нитрифицирующие бактерии, а также на серо- и железобактерии.
Данная статья будет посвящена наиболее распространенной среди них группе - нитрофицирующим бактериям.
История открытия
Еще в середине 19 века немецкими учеными было доказано, что процесс нитрификации является биологическим. Опытным путем они показали, что при добавлении к канализационным водам хлороформа останавливалось окисление аммиака. Но объяснить, почему так происходит, они не смогли.
Это удалось сделать несколькими годами позже русскому ученому Виноградскому. Он выделил две группы бактерий, которые поэтапно брали участие в процессе нитрификации. Так, одна группа обеспечивала окисление аммония до кислоты азотистой, а уже вторая группа бактерий отвечала за ее превращение в азотную. Все задействованные в этом процессе нитрифицирующие бактерии являются грамотрицательными.
Особенности процесса окисления
Процесс образования нитритов путем окисления аммония имеет несколько этапов, в ходе которых образуются азотсодержащие соединения с различной степенью окисленности группы NH.
Первым продуктом окисления аммония является гидроксиламин. Вероятней всего, он образуется из-за включения молекулярного кислорода в группу NH 4 , хотя окончательно этот процесс не доказан и остается дискутабельным.
Далее гидроксиламин превращается в нитрит. Предположительно, процесс осуществляется через образование NOH (гипонитрита) с выделением закиси азота. В этом случае ученые считают продукцию закиси азота всего лишь побочным продуктом синтеза, из-за восстановления нитрита.
Кроме продукции химических элементов, в ходе денитрофикации выделяется большое количество энергии. Подобно происходящему у гетеротрофных аэробных организмов, в данном случае синтез молекул АТФ связан с окислительно-восстановительными процессами, в результате которых на кислород передаются электроны.

При окислении нитрита большую роль играет процесс обратного транспорта электронов. Включение его электронов в цепь происходит непосредственно в цитохромах (С-типа и/или А-типа), а для этого требуется достаточно большие затраты энергии. Как результат, хемоавтотрофные нитрифицирующие бактерии полностью обеспечены нужным запасом энергии, которая используется для процессов построения и усвоения углекислоты.
Виды нитрифицирующих бактерий
В первой фазе нитрификации берут участие четыре рода нитробактерий:
- нитросомонас;
- нитроцистис;
- нитросолюбус;
- нитрососпира.
Кстати, на предложенном изображении вы можете видеть нитрифицирующие бактерии (фото под микроскопом).

Экспериментальным путем среди них достаточно сложно, а зачастую и вовсе невозможно выделить одну из культур, поэтому их рассмотрение преимущественно комплексное. Все из перечисленных микроорганизмов имеют размер до 2-2,5 мкм и преимущественно овальную или округлую форму (за исключением нитроспиры, которые имеют вид палочки). Они способны к бинарному делению и направленному движению за счет жгутиков.
Во второй фазе нитрификации принимают участие:
- род нитробактер;
- род нитроспина;
- нитрококус.
Наиболее изучен штамм бактерий рода нитрбактер, имеющий название в честь своего первооткрывателя Виноградского. Эти бактерии нитрифицирующие имеют грушевидную форму клеток, размножаются почкованием, с образованием подвижной (за счет жгутика) дочерней клетки.
Строение бактерий
Исследованные нитрифицируюшие бактерии имеют схожее клеточное строение с другими грамотрицательными микроорганизмами. Некоторые из них имеют достаточно развитую систему внутренних мембран, образующих стопку в центре клетки, тогда как у других они располагаются больше по периферии или образуют структуру в виде чаши, состоящую из нескольких листков. По всей видимости, именно с этими образованиями связаны ферменты, которые участвуют в процессе окисления нитрификаторами специфических субстратов.
Тип питания нитрифицирующих бактерий
Нитробактерии относятся к облигатным автотрофам, поскольку не способны использовать экзогенные органические вещества. Однако экспериментальным путем все же показана способность некоторых штаммов нитрифицирующих бактерий использовать некоторые органические соединения.
Было выявлено, что субстрат, содержащий дрожжевые автолизаты, серин и глутамат в низких концентрациях, стимулирующим образом воздействовал на рост нитробактерий. Это происходит как при наличии нитрита, так и при его отсутствии в питательной среде, хотя процесс протекает гораздо медленнее. И наоборот, при наличии нитрита процесс окисления ацетата подавляется, но значительно увеличивается включение его углерода в белок, различные аминокислоты и другие клеточные компоненты.
В результате множественных экспериментов были получены данные о том, что бактерии нитрифицирующие все же могут переключаться на гетеротрофное питание, но насколько продуктивно и как долго они могут существовать в таких условиях, еще предстоит выяснить. Пока данные достаточно противоречивы, чтобы делать окончательные умозаключения по этому поводу.
Среда обитания и значение нитрифицирующих бактерий
Нитрифицирующие бактерии относятся к хемоавтотрофам и имеют широкое распространение в природе. Они встречаются повсеместно: в почве, различных субстратах, а также водоемах. Процесс их жизнедеятельности вносит большой вклад в общий круговорот азота в природе и в действительности может достигать огромных масштабов.

Например, такой микроорганизм, как нитроцистис океанус, выделенный из Атлантического океана, относится к облигатным галофилам. Он может существовать только в морской воде или субстратах, содержащих ее. Для таких микроорганизмов важна не только среда обитания, но и такие константы, как рН и температура.
Все известные нитрифицирующие бактерии относят к облигатным аэробам. Для того чтобы окислить аммоний в азотистую кислоту, а азотистую кислоту в азотную, им нужен кислород.
Условия обитания
Еще одним важным моментом, который выявили ученые, стало то, что место, где живут нитрифицирующие бактерии, не должно содержать органических веществ. Была выдвинута теория, что эти микроорганизмы в принципе не могут использовать органические соединения из вне. Их даже назвали облигатными автотрофами.
В последующем неоднократно было доказано пагубное влияние глюкозы, мочевины, пептона, глицерина и другой органики на бактерии нитрифицирующие, но эксперименты не останавливаются.
Значение нитрифицирующих бактерий для почвы
До недавнего времени считалось, что нитрификаторы благоприятно влияют на почву, увеличивая ее плодородность путем расщепления аммония до нитратов. Последние не только хорошо абсорбируются растениями, но и сами по себе повышают растворимость некоторых минеральных веществ.
Однако, в последние годы научные взгляды претерпевают изменения. Выявлено отрицательное действие описываемых микроорганизмов на плодородность почвы. Бактерии нитрифицирующие, образуя нитраты, подкисляют среду, что не всегда является положительным моментом, а также в большей степени провоцируют насыщение почвой ионов аммония, чем нитратов. Более того, нитраты имеют способность восстанавливаться до N 2 (в процессе денитрифакации), что в свою очередь ведет к обеднению почвы азотом.

В чем опасность нитрифицирующих бактерий?
Некоторые штаммы нитробактерий в присутствии органического субстрата могут окислять аммоний, образовывая гидроксиламин, а в последующем нитриты и нитраты. Также в результате таких реакций могут возникать гидроксамовые кислоты. Более того, ряд бактерий осуществляет процесс нитрификации различных соединений, в состав которых входит азот (оксимы, амины, амиды, гидроксаматы и другие нитросоединения).
Масштабы гетеротрофной нитрификации при определенных условиях могут быть не только огромными, но и весьма пагубными. Опасность заключается в том, что в ходе таких превращений происходит образование токсических веществ, мутагенов и канцерогенов. Поэтому ученые пристально работают над изучением данной темы.
Биологический фильтр, который всегда под рукой
Нитрифицирующие бактерии - это не абстрактное понятие, а весьма распространенная форма жизни. Более того, они часто используются человеком.
Например, в состав биологических фильтров для аквариумов входят именно эти бактерии. Данный вид очистки менее затратный и не такой трудоемкий, как механическая очистка, но в тоже время требует соблюдения определенных условий, чтобы обеспечить рост и жизнедеятельность нитрифицирующим бактериям.
Наиболее благоприятным микроклиматом для них является температура окружающей среды (в данном случае воды) порядка 25-26 градусов Цельсия, постоянный приток кислорода и наличие водных растений.

Нитрифицирующие бактерии в сельском хозяйстве
Для того чтобы повысить урожайность, аграрии используют различные удобрения, содержащие нитрифицирующие бактерии.
Питание почвы в таком случае обеспечивается нитробактериями и азотобактериями. Эти бактерии извлекают из почвы и воды необходимые вещества, которые в процессе окисления образуют достаточно большое количество энергии. Это так называемый процесс хемосинтеза, когда полученная энергия идет на образование сложных молекул органического происхождения из углекислого газа и воды.
Для этих микроорганизмов не обязательно поступление питательных веществ с окружающей их среды - они могут продуцировать их самостоятельно. Так, если зеленым растениями, которые также являются автотрофами, необходим солнечный свет, то для нитрифицирующих бактерий он не обязателен.
Самоочистка почвы
Почва - это идеальный субстрат для роста и размножения не только растений, но и множества живых организмов. Поэтому крайне важно ее нормальное состояние и сбалансированный состав.
Следует помнить, что биологическую очистку почвы обеспечивают в том числе и нитрифицирующие бактерии. Они, находясь в почве, водоемах или перегное, превращают аммиак, который выделяют другие микроорганизмы и отходные органические материалы, в нитраты (если быть более точными, то в соли азотной кислоты). Весь процесс состоит из двух этапов:
- Окисление аммиака до нитрита.
- Окисление нитрита до нитрата.
При этом каждый этап обеспечивается отдельными видами микроорганизмов.
Так называемый замкнутый круг
Кругооборот энергии и поддержание жизни на Земле возможно благодаря соблюдению определенных закономерностей существования всего живого. На первый взгляд трудно понять, о чем идет речь, но на самом деле все достаточно просто.

Давайте представим следующую картинку из школьного учебника:
- Неорганические вещества перерабатываются микроорганизмами и тем самым создают благоприятные условия в почве для роста и питания растений.
- Они, в свою очередь, являются незаменимым источником энергии для большинства травоядных животных.
- Следующей цепочкой этого жизненного звена являются хищники, энергией для которых являются, соответственно, их травоядные собратья.
- Люди, как известно, относятся к высшим хищникам, а это значит, что мы можем получать энергию как от растительного мира, так и от животного.
- А уже наши собственные остатки жизнедеятельности, а также тех самых растений и животных, служат питательным субстратом для микроорганизмов.
Таким образом, получается замкнутый круг, непрерывно функционирующий и обеспечивающий жизнь всего живого на Земле. Зная эти принципы, не сложно представить, насколько многогранна и на самом деле безгранична сила природы и всего живого.
Заключение
В данной статье мы попытались дать ответ на вопрос, что такое нитрифицирующие бактерии в биологии. Как видите, несмотря на неопровержимые доказательства жизнедеятельности, функционирования и влияния этих микроорганизмов, существует еще множество спорных вопросов, требующих дальнейших экспериментальных исследований.
Нитрифицирующие бактерии относят к хемотрофам. Источником энергии для них служат различные минеральные вещества. Несмотря на свои микроскопические размеры, эти живые организмы оказывают огромное влияние на окружающий их мир.
Как известно, хемотрофы не могут усваивать органические соединения, которые находятся в субстрате (почвенном или водном). Они, наоборот, продуцируют строительный материал для создания живой и функционирующей клетки.
Живые организмы по типу питания подразделяются на автотрофы и гетеротрофы. Последние самостоятельно строят новые элементы из углекислоты и других неорганических веществ. Нитрифицирующие бактерии являются известной формой жизни, часто использующейся в быту и хозяйстве. Эти виды входят в состав очищающих устройств для аквариумов.
Нитрифицирующие бактерии используются для очистки аквариума
Основная характеристика
Источники энергии, поддерживающие условия жизни организмов, определяют их деление на фотоавтотрофы и хемоавтотрофы, которые зависят от солнечной энергии и минеральных компонентов. В зависимости от окислителя хемоавтотрофа, выделяют водородные и нитрифицирующие бактерии, серо- и железобактерии.
Предназначение и классификация
В начале XIX века ученые доказали, что нитрификация относится к биологии. Для этого к сточным водам они добавляли хлороформ.
Среди автотрофов, производящих сложную органику из простых неорганических молекул, известны организмы, применяющие энергию. Это водоросли, бактерии, вырабатывающие органические вещества из углекислого газа и воды. Присутствие автотрофов обусловлено наличием кислорода и невысокой влажностью.
 Нитрифицирующие бактерии имеют большое значение в сельском хозяйстве
Нитрифицирующие бактерии имеют большое значение в сельском хозяйстве Организмы, принимающие энергию от окисления и восстановления (хемоавтотрофы), выявлены среди бактерий. По физиологическим, биологическим и химическим свойствам и значению эти микроскопические организмы представляют интерес для отдельных сфер сельского хозяйства.
Во время исследования завершался процесс окисления аммиака. Виноградский разделил нитрификаторы на бактерии, исполняющие первый этап этого процесса (окисление аммония до азотистой кислоты), и второй - переход этой кислоты в азотную. Грамотрицательные бактерии относятся к нитробактериям.
Представители первой фазы Nitro:
- Somonas (Сомонас);
- Socystis (Сосайстис);
- Solobus (Солобус);
- Sospira (Соспира).
Больше изучен вид Сомонас, хотя создание настоящих культур представляется сложным. Клетки овальной формы, размножаются образованием дочерних прокариотов из материнской клетки. В результате развития микроорганизмов в жидкой среде имеются подвижные формы с несколькими жгутиками и недвижимой зооглеей.
Нитрососайстис характеризуются круглой формой, размером до 2 мкм. Некоторые представители достигают 10 мкм. Передвигаются благодаря одному жгутику, образуют зооглеи и цисты. Нитросолобус равен 1−1,5*1−2,5 мкм. Клетки делятся на части, и поэтому внешняя форма неправильная.
Клетки Nitrosospira палочковидные или извивающиеся, размером 0,9−1*1,5−2,60 мкм, имеют до 5 жгутиков.
 Бактерии имеют размер 0,9−1*1,5−2,60 мкм
Бактерии имеют размер 0,9−1*1,5−2,60 мкм Бактерии второй фазы Nitro:
- Bacter (Бактер);
- Spina (Спина);
- Coccus (Кокус).
Пагубное влияние органических веществ на хемоавтотрофные организмы отмечено и в исследованиях ученых. Они не применяют экзогенные органические элементы и называются облигатными автотрофами. Применять отдельные соединения бактерии могут с ограниченными возможностями.
Улучшается рост Нитробактер при наличии нитрита дрожжевого автолизата, пиридоксина, глутамата и серина, если они в слабой концентрации вносятся в среду.
Основное строение нитрификаторов:
- Сформированная система мембран в виде стопки в центре клетки, посередине.
- Чашеподобная структура, состоящая из нескольких листиков.
Клетки Nitrobacter по виду напоминают грушу. Размножаются путем почкования. Информация о бактериях Нитроспина и Нитрококус ограничена.
По строению клеток изученные бактерии аналогичны другим грамотрицательным микроорганизмам. У некоторых есть сформированные системы внутренних мембран, создающих стопку в середине клетки (Нитрососайстис), размещаются параллельно мембране цитоплазме (Нитросомонас) или формируют чашеподобную структуру из слоев (Нитробактер Виноградский). Кислород важен для окисления аммония в азотную кислоту:
 По строению клеток изученные бактерии аналогичны другим грамотрицательным микроорганизмам
По строению клеток изученные бактерии аналогичны другим грамотрицательным микроорганизмам Нитробактер и Нитросомонас воссоздают нитриты с аммонием. Наряду с нитрифицирующими хемотрофами существуют гетеротрофы, имеющие похожие процессы. К ним относятся грибы из рода Фусамм и бактерии Алкалигенес, Соринебактериум, Ахромоба-ктер, Псеудомонас, Арфробактер. Нокардиа окисляет аммоний с созданием гидроксиламина, нитритов и нитратов. В итоге образуется гидроксамовая кислота.
Азот является важным элементом, входящим в состав нуклеиновой кислоты и белка. Величины гетеротрофной нитрификации огромные. Создаются продукты с токсичным, ядовитым, канцерогенным, мутагенным действием и с химиотерапевтическим эффектом. По этой причине изучению процесса и выяснению его значения для гетеротрофных культур уделено большое внимание.
Образование химических соединений для создания энергии является хемосинтезом, благодаря которому растут и развиваются клетки. Хемоавтотрофные типы распространены в природе и наблюдаются в почве и водоемах. Производимые ими процессы совершаются в огромных масштабах и имеют важнейший смысл в круговороте азота.
Ученые прошлого века считали, что производительность нитрификаторов обогащает почву, поскольку они трансформируют аммоний в нитраты, которые легко всасываются растениями, а также увеличивают усвоение минералов. Растения, усваивая аммонийный азот и ионы аммония, лучше хранятся в почве, чем нитраты. Образовавшиеся нитраты подкисляют среду обитания, обедняют состав почвы по количеству азота.
Питание микроорганизмов
Бактерии нитрификаторы являются автотрофами, так как не используют экзогенные органические вещества. Основа с дрожжевым аутолизатом, серином и глутаматом в низкой концентрации влияет на рост бактерий. Это происходит из-за нитрита, находящегося в питательной среде. Окисление ацетата сокращается, но возрастает добавление его углерода в белок, аминокислоты и прочие компоненты.
В результате проведенных исследований получена информация о том, что бактерии переходят на гетеротрофное питание.
Среда обитания и опасность
Нитрифицирующие бактерии распространены в окружающей среде. Они присутствуют в грунте, разных субстратах и водоемах. Процесс их функционирования вносит существенный вклад в общий этап движения азота в природе.
Нитрификаторы обитают в простой минеральной среде, содержащей окисляемый субстрат в виде аммония, нитритов и углекислоты.
 Нитрифицирующие бактерии довольно распространены в окружающей среде
Нитрифицирующие бактерии довольно распространены в окружающей среде В окружающем мире микроорганизмы обрабатывают неорганические вещества и создают условия для питания растений в грунте. Источником энергии для животных является флора. Человек питается растениями и животными. Остатки жизнедеятельности флоры и фауны служит пищей для бактерий. Круговорот замыкается.
Такой микроорганизм, как Нитрососайстис, выделен из вод Атлантики. Он относится к облигатным галлофилам и обитает в соленой среде. Уровень pH (реакция водорода) для роста бактерий равен 8,7, а оптимальное значение составляет 7,5.
Среди вида Сомонас распространены типы, имеющие температурный режим при 26 или около 40 °C, и штаммы, быстрорастущие при 4 °C. Благоприятным климатом является среда обитания (вода) 24−27 градусов. Должен быть устойчивый доступ кислорода и наличие водной растительности.
Простейшие бактерии относят к облигатным аэробам. Для окисления аммония в азотистую кислоту, а азотистой кислоты в азотную им необходим кислород. Место обитания не должно содержать органических соединений. В исследованиях подтверждено губительное действие глюкозы, гербицидов, мочевины, пептона, глицерина и другой органики на бактерии.
 Простейшие бактерии относят к облигатным аэробам, тк им нужен кислород для переработки аммония
Простейшие бактерии относят к облигатным аэробам, тк им нужен кислород для переработки аммония Некоторые штаммы нитробактерий при наличии органического составляющего окисляют аммоний, создавая гидроксиламин, нитриты и нитраты. Вследствие таких реакций появляются гидроксамовые кислоты. Бактерии выполняют процесс нитрификации разных соединений, в состав которых входит азот.
Объемы гетеротрофной нитрификации при особых обстоятельствах могут быть губительными. Опасность состоит в том, что образуются токсины, мутагены и канцерогены.
Применение в различных сферах
Использование в различных областях нитрифицирующих бактерий вносит свои достоинства и недостатки. Микроорганизмы создают благоприятные условия для обитания рыб в аквариуме, обогащения почвы, а также сельскохозяйственных процессов.
Биологический фильтр для аквариума
Нитробактерии играют важную роль в превращении токсического аммиака в нитраты. Это важно при запуске нового аквариума. Эти микроорганизмы составляют небольшую долю бактерий и являются биофильтром. Они размножаются на любой поверхности (наполнитель фильтра, грунт или растения). Если водорослей в аквариуме находится большое количество, тогда аквариум полностью считается биофильтром. Важно создать благоприятную обстановку для размножения полезных бактерий.
 Нитробактерии превращают токсический аммиак в нитраты
Нитробактерии превращают токсический аммиак в нитраты Сократить популяцию бактерий в аквариуме могут дефицит кислорода, избыток углекислоты, снижение pH и использование дезинфекторов. Нитрифицирующие бактерии растений лишают питания водорослей. Живые бактерии для аквариума применяются во время подготовки резервуара к использованию.
Важность микроорганизмов велика , ведь они очищают воду от загрязнений, биологических и органических остатков, отложений и испражнений. Поэтому микрофлора в резервуарах, где они обитают, идеальная.
Нитрифицирующие бактерии - главные очистители обитаемых помещений с рыбками и моллюсками. Они активно размножаются в среде, насыщенной аммонием, нитритами, азотом и аммиаком.
Для запуска аквариума используются препараты марки «Сера», содержащие в составе живые нитрификаторы и вулканическую пыль - безупречную среду для скорейшего размножения и роста. Этот субстрат оседает на дно и становится частью грунта. В аквариум заселяются сразу несколько бактерий.
Большая часть продукции, поставляемой в специализированные зоомагазины, содержит культуры гетеротрофных бактерий.
Значение для сельского хозяйства
С целью повышения урожайности аграрии применяют всевозможные удобрения, содержащие нитрифицирующие бактерии.
Почва является идеальным субстратом для процессов роста, размножения растений и живых организмов, поэтому важно поддерживать ее правильное содержание и комплексный состав.
Биологическую обработку грунта проводят природные чистильщики - нитрифицирующие бактерии. Для них не обязателен доступ веществ из внешней среды - они могут вырабатывать их автономно. Например, автотрофным зеленым растениям нужен солнечный свет, а для нитробактерий безразличен.
Присутствуя в почве, перегное или водной среде, они превращают выделяемый аммиак в нитраты (соль азотной кислоты). Каждый этап проводится с помощью разных бактерий.
 Биологическую обработку грунта проводят природные чистильщики - нитрифицирующие бактерии.
Биологическую обработку грунта проводят природные чистильщики - нитрифицирующие бактерии. Процесс перехода аммиака в нитраты:
- Окисление аммиака до нитрита. Этот процесс происходит не одним типом бактерий, а разными. Одни виды микроорганизмов превращают в нитрит, а другие - в нитрат. Важным условием должна быть температура от 4 градусов, влажность и обилие кислорода.
- Окисление нитрита в нитрат.
Нитрификаторы положительно влияют на почву, повышая ее плодородность за счет расщепления аммония. Однако учеными выявлено также негативное влияние. Бактерии подкисляют почву, что не является благоприятным моментом, а также насыщают почву ионами аммония. Впоследствии почва истощается по количеству полезных веществ.
Энергетическим источником для хемотрофов являются разнообразные минеральные вещества. Экосистема создается искусственно, но для удачного развития запускают установленные процессы, регулировкой которых занимаются жители резервуара, например, аквариума.
Несмотря на крошечные размеры, эти живые организмы влияют на окружающий мир. Нитробактерии распространены в почвах, морской и пресной воде, играют важную роль в переработке сточных вод.